المجرات، النجوم، الكواكب، الأقمار، الشُهب، النيازك، الكائنات الحية، وكُلُ شيء في هذا الكون يتكون من وحدات مُتناهية الصِغَر تُعرَف بالذرات. تلك الذرات هي التي تُعْزَى إليها خواص المادة الكيميائية والفيزيائية، ويرجع أصل كلمة ذرة إلى كلمة ”أتوموس” في اللغة الإغريقية، والتي تعني غير القابل للإنقسام؛ إذ كان يُعتَقَد أنه ليس هناك ما هو أصغر من الذرة. (وهل يوُجد ماهو أصغر من الذرة؟)*
وقد قدَّم فلاسفة الإغريق من القرن الخامس قبل الميلاد أولى الإفتراضات بخصوص الذرة، فمثلًا افترض “ديموقريطس” أن لكُل ذرة شكل مُحدَّد كالحصوات الصغيرة، وهذا الشكل هو ما يحكُم خواص تلك الذرة، وجاء ارسطو الذي استنكر فكرة ديموقريطس عن الذرة، وللأسف ظلت أفكار أرسطو منتشرة حوالي ألفي عام؛ أثناء ذلك كادت فكرة ديموقريطس أن تكون قد اختفت!
لكن بالطبع فقد مَرَّت البنية الذرية بعد ذلك بعديد من النماذج والتَطَوُرات حتى وصلت لما نعرفُه عنها اليوم.
الذرة: من ثومبسون إلى دالتون
نموذج دالتون (بداية القرن السابع عشر)

دالتون
اعتمد العالِم جون دالتون في تفسير نموذجه عن الذرة على قوانين بقاء الكُتلة*1 والنِسَب الثابتة؛ عن طريق تجاربه وأبحاثه. على سبيل المثال: دراسته لتأثير الضغط على الغازات، وبحثه عن خصائص المُركبَّات والذي أوضَّح فيه:- ديمومة وجود عناصر أنقى تكون المُركبّات بنفس النسبة، وفي حالات اُخرى تتكون من عناصر مُختلفة بنسب مُختلفة. ومِن ثَم استنتَج أن هذه العناصر لابُد أن تتكون من وحدات/جُسيمات أصغر تتحد او ترتبط مع بعضها بطُرق شتى.
وجاءت فروض وتصورات دالتون عن الذرة كالآتي: المواد تتكون من العديد من الذرات وهذه الذرات جُسيمات دائرية صغيرة جداً غير قابلة للتجزئة، كما أن ذرات العُنصر الواحد مُتشابهة الخواص، بينما تختلف ذرات العناصر المختلفة. التغيُّر في توزيع الذرات يُعَّرَف على أنه إتحادٌ الكيميائي، كما يُمكن لذرات العناصر المختلفة أن تتحد مع بعضها. وجديرٌ بالذِكرِ أن نموذج دالتون أثبت نجاحه بتفسير بعض الحقائق والتنبوء ببعض القوانين مثل قانون النِسَب المُتعدِّدَة*2 (النسب المتضاعفة)، وهو قانون يحكُم إتحاد ذرات المواد المُختلفة وعلاقة تكوُّن المُركبات بنسِب الأوزان الذرية لهذه المواد.
الكُتلة(المادة) لا تفنى ولا تُستَحدث من العَدم. فمثلاً عندما يتفاعل حامض الهيدروكلويك (يحتوي على ذرتين: أحدُهما كلور والأُخرى هيدروجين) مع هيدروكسيد الصوديوم (يحتوي ثلاث ذرات: صوديوم، أُكسجين وهيدروجين)؛ لابُد أن تكون نواتج التفاعُل تحتوي بالضبط نفس الخمس ذرات السالِف ذكرهم.
|
قانون بقاء الكُتلة | |
قانون يكشف كينونة التفاعلات الكيمائية؛ حيث يخبرنا أنه عند اتحاد عنصرين وتكوين مُركَّب واحد؛ فإن النسبة بين الكُتل المُختلفة من أحد العُنصرين التي تتحد مع كُتلة ثابتة من العُنصر الآخر، تكون نسبية عددية صحيح (1 أو 2 أو 3…)
|
قانون النِسَب المُتعدِّدَة |

نموذج دالتون الذري
ذرة فاراداي
توصَّل العالِم مايكل فاراداي إلى أن الذرات تحتوي على جُسيمات كهربية تُسَمَّى إلكترونات، وقام بعمل تجارب التحليل الملحي (التحليل الكهربي)، إلا أنه لم يضع أي نموذج ذري.

مايكل فاراداي
نموذج طومسون (عام 1897)

جوزيف جون طومسون
أجرى العالِم جوزيف جون طومسون أبحاثاً شهيرة حول خصائص أشعة الكاثود (التي أثبتت أن التيار الكهربي يتكون من تدفُق جُسيمات سالبة الشُحنة، على عكس ما كان سائداً حينها بأن التيار الكهربي يتكون من أشعة تُشبه أشعة الضوء)، ثُم في أبريل عام 1897 أعلَّن إكتشاف الإلكترون وخصائصه، ومِن ثَمَّ جاء السؤال الصعب “إذا كانت الإلكترونات سالبة الشُحنة فكيف تكون الذرة مُتعادلة كهربياً؟”،بمعنى آخر: أين هي الشُحنة الموجبة التي تُعادل شُحنة الإلكترون؟
كانت الإجابة تكمُن في تحطيم المفهوم القديم عن الذرة الذي سيطر على الوسط العلمي حوالي ألفي عام، والذي ينطوي على أن الذرة غير قابلة للتجزئة وبعد تقديم عدة تفسيرات باءت بالفشل من قِبَل عُلماء كُثُر حينذاك، قدَّم طومسون التفسير السليم وهو أن الذرة كُرة من الشحنات المُوجبة تتخللُها إلكترونات سالبة وبذلك تكون الذرة مُتعادلة كهربياً. وجديرُ بالذكرِ أن عمل طومسون قد قدَّم الكثير من البراهين العلمية للمُجتمَع العلمي حول البُنَى الذرية في عصره.
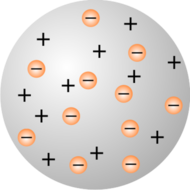
نموذج طومسون الذري
الذرة بين رذرفورد وبور
نموذج رذرفورد عن الذرة (النموذج النووي عام 1911)

ارنست رذرفورد
تصوَّر العالِم ارنست رذرفورد في نموذجه عن الذرة أنها بمُعظمها فراغ، ويُوجَد في مركزها نواة صغيرة جداً موجبة الشحنة، وتلك النواة كثيفة نسبياً -تتركز فيها مُعظم كتلة الذرة-، لكن النواة صغيرة جداً مُقارنةً بالذرة. كما يوجد جُسيمات ضئيلة جداً سالبة الشحنة تدور حول النواة وتُعرَف بالالكترونات.
وجاءت تصورات رذرفورد عن الذرة أن كُتلتها تُعَدُّ تعبيراً عن مجموع كُتل البروتونات في النواة مع إهمال كُتل الإلكترونات؛ إذ أنها ضيئلة للغاية. كما أن النواة ذات شحنة موجبة نسبةً إلى شنحة البروتونات الموجبة وتتوزع الإلكترونات في الذرة حول النواة بنفس طريقة توزُّع الأجرام السماوية حول الشمس حيث تأخذ مدارات مُحدَّدَة، ولأن الذرة مُتعادلة كهربياً فإن عدد البروتونات يُكافئ عدد الإلكترونات. وقد قام رذرفورد بعدة تجارب شهيرة من أجل الوصول إلى حقائق أكثر عن البنية الذرية.

نموذج رذرفورد الذري
نموذج بور عن الذرة (عام 1913)

نيلز بور
اعتمد تصوَّر العالِم نيلز بور في نموذجه الذري على تصورات رذرفورد من حيث أن الإلكترونات تدور حول النواة في مدارات مُحَدَّدة ثابتة، أَطلَق عليها مُصطلح مستويات الطاقة. كما أن لكُل مستوى طاقة عدد مُحدَّد من الإلكترونات يشغله لا يزيد عنه، والفراغ الموجود بين مستويات الطاقة هو بمثابة مناطق مُحرَّمة على الإلكترونات أن يتواجدوا فيها. أيضاً لا يفقد الإلكترون أى طاقة طالما هو في مستوى طاقته الخاص، لكن في حين إكتسابه طاقة (طاقة طيف الامتصاص) فإنه ينتقل إلى مستوى طاقة أعلى لكن سُرعان ما يفقد هذه الطاقة على هيئة شُعاع ضوء (طيف إنبعاث) ويعود إلى مستوى طاقته مرة اُخرى.
وقد نجح بور بهذه الإفتراضات في أن يفسر الترددات والأطوال الموجية المُحَدِّدَة للطيف الخطي المُنبَعِث من الذرات، كما ساعد نموذج بور في تفسير كيفية تفاعل الذرات مع الضوء والأشكال الاُخرى للإشعاع. كما وقد ساعد الكيميائيين في الحصول على الكثير من المعلومات حول تركيب الجُزيئات عن طريق قياس كمية الإشعاع المُمتَصَة والمُنبَعثَة.
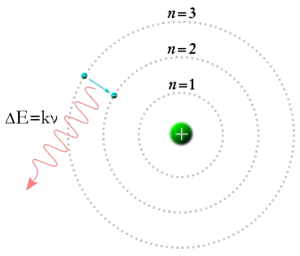
نموذج بور الذري
النموذج الذري الحديث والنموذج الذري الكمَّي
النموذج الذري الحديث
تتكون الذرة من نواة تحتوي على شحنات موجبة تتمثل في البروتونات. تتركز مُعظم الكتلة في النواة مُحاطة بإلكترونات سالبة الشحنة وتتحرك بسرعة كبيرة ولها خواص الموجات وموجودة في فراغ حول النواة يكون احتمال وجودها فيه أكثر من 90% ويُسَمَى هذا الفراغ بالمجالات الإلكترونية.
النموذج الكمي للذرة (تفسير ميكانيكا الكم)
تتكون الذرة من سحابة من شحنات سالبة تتمثل في الإلكترونات وتحوم هذه الإلكترونات حول نواة صغيرة جداً في المركز وتتكون النواة من بروتونات موجبة الشحنة، ونيوترونات متعادلة. كما أن الذرة هي أصغر جزء من العنصر يمكن أن يتميز به عن بقية عناصر الطبيعة ، حيثُ كلما غصنا أكثر في المادة كلما وجدنا البُنى الأصغر التي لا تجعل فرقاً بين عنصر وآخر. أيضاً الذرة بما تحمله من خصائص تُحَدِّدُ الفروق الجوهرية بين العناصر المختلفة، وكذلك تحديد قابلية عنصر ما لدخول تفاعل كيميائي من عدمه.
النظرية الموجية
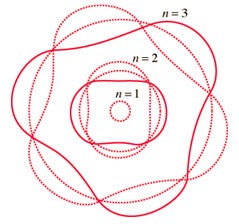
نموذج النظرية الموجية للذرة
إن أكثر النظريات التي لاقت قبولاً في تفسيرها للبنية الذرية هي النظرية الموجية، والتي بُنيَت تصوراتها على تصورات نموذج بور الذري مع الأخذ في الإعتبار الاكتشافات الحديثة والتَّطَوُرات في ميكانيكا الكم.
في عام 1926 وضع العالِم ارفين شرودنغر معادلة موجية تُعرَف بالدالة الموجية أو معادلة شرودنجر، كما استبدل مفهوم المدار الإلكتروني بالأوربيتال حتى يكون النموذج الذري أكثر موضوعية وتعبيراً عن البنية الذرية. وفروض النظرية الموجية تلخَصَت في الآتي: مُعظم الفراغ الذري مشغول بالأوربيتالات التي تحتوي على الإلكترونات، وكُل أوربيتال يتسع لإلكترونين يتم الحُكْم عليهم من خلال ثلاث أعداد كمية (عدد الكم الرئيسي، عدد الكم الثانوي، عدد الكم المغناطيسي)، بالإضافة لكون الإلكترون في أي أوربيتال له قيمة واحدة من عدد الكم المغزلي وهو عدد الكم الرابع. كما أن هذه الأوربيتالات ليست ثابتة وإنما تُمَثِل إمكانية تواجُد إلكترونين لهم نفس أعداد الكمية الثلاث، ويُمكن الحُكم على آخر حدود كُل أوربيتال عندما يقل تواجد الإلكترون في منطقةٍ ما عن 90%.
ارفين شرودنجر
مكونات الذرة
– الإلكترونات: هي جُسيمات سالبة الشُحنة ذات كُتلة ضئيلة جداً تساوي تدور حول النواة بسرعة فائقة. وقد اكتشف العالِم طومسون الإلكترون عام 1917.
– البروتونات: هي جُسيمات موجبة الشحنة ذات كُتلة أكبر كثيراً من الإلكترونات (كتلة البروتون = 1800 مرة كُتلة الإلكترون)، كما لها سُرعة دوران فائقة حول النواة. وقد اكتشف العالِم رذرفورد البروتون عام 1919 ويتكون البروتون من ثلاث كواركات ( كوارك سُفلي و 2 كوارك علوي)، والكوارك هو جُسيم أصغر بكثير من البروتون وله شُحنة ولكنها تُنسَب لشحنة الإلكترون حيث تأخذ قيم سالب ثُلث شحنة الإلكترون و ثُلُثي شحنة الإلكترون ويبلغ عدد الكواركات المعروفة ستة أنواع (القاعي – الغريب – السُفلي – القمي – الساحر – العلوي)
– النيوترونات: هي جُسيمات مُتعادلة الشحنة ذات كُتلة تُقارب كُتلة البروتونات ولها أيضاً سرعة فائقة. وقد اكتشف العالِم/ شادويك النيوترونات عام 1932 ويتكون النيوترون من ثلاث كواركات (كوارك علوي و 2 كوارك سُفلي)
– النواة: هي جُزء ضئيل جداً تتركز فيه مُعظم كُتلة الذرة ولها جاذبية هائلة بحيث تُبقى جميع الجُسيمات في حركة دائمة وسريعة حولها.
ويلزم لوصف نواة الذرة معرفة ماهية العددي الكُتلي والعدد الذري وعدد النيوترونات.
العدد الكُتلي (A) : مجموع أعداد البروتونات والنيوترونات داخل نواة الذرة
ويُطلَق على البروتونات والنيوترونات داخل النواة مُصطَلَح النيوكلونات
العدد الذري (Z): عدد البروتونات داخل النواة = عدد الإلكترونات [في الذرة المُتعادلة]
عدد النيوترونات (N): العدد الكُتلي مطروحٌ منه عدد البروتونات.
النظائر
النظائر هي ذرات العُنصر الواحد التي تتفق في عددها الذري ولكن تختلف في عددها الكُتلي، وذلك لاختلاف عدد النيوترونات داخل أنوية الذرات. وهي تتفق في الخواص الكيميائية لأنها في الأصل تتفق في العدد الكُلي للإلكترونات وترتيبها حول النواة، كما أن مُعظم عناصر الجدول الدوري لها أكثر من نظير.
والنظائر نوعان:
ـ النوع الأول: الأيزوبارات وهي ذرات العناصر التي تختلف في العدد الذري ولكنها تتفق في العدد الكُتلي
ـ النوع الثاني: الأيزوتونات وهي ذرات العناصر التي تختلف في العدد الكُتلي ولكنها تتفق في عدد النيوترونات
وكثيرةٌ هي الأمثلةُ على النظائر وأنواعها فمثلاً نظائر الهيدروجين:
1ـ البروتيوم: ذرة هيدروجين بها إلكترون واحد وبروتون واحد
2ـ الديوتيريوم: ذرة هيدروجين بها إلكترون واحد وبروتون ونيوترون
3ـ التريتيون: ذرة هيدروجين بها إلكترون واحد وبروتون ونيوترونان إثنان
لكن هل يُمكن حساب كُتلة الذرة؟، وما علاقة الكُتلة بالطاقة؟
إن كُتلة الذرة ضئيلة جداً، ولذلك تُقَدَّر بوحدة الكُتل الذرية وتساوي من الكيلو جرام 1.66 ضرب 10 مرفوعة لأُس ناقص 27
ويتراوح عدد الذرات بالكون من (4 ضرب 10 مرفوعة لأُس 78) إلى (6 ضرب 10 مرفوعة لأُس 79) ذرة، وقد تمت هذه الحسابات تبعاً لنظرية التضخُم الكوني، وسواء أكان الكون لانهائي أم لا فإن هذا لايتنافي مع هذه الحسابات؛ إذ أن الكون الخاضِع للدراسة يقع ضمن نطاق 13.8 مليار سنة (عُمر الكون من لحظة الإنفجار العظيم).
وقد وضع عالِم الفيزياء الشهير ألبرت آينشتين مُعادلة رياضية توضح العلاقة بين الكُتلة المُتحوّلة والطاقة، بحيث يُمكن حساب الطاقة الناتجة عن تحول الكُتلة (مُقدرة بالكيلو جرام أو بوحدة الكُتل الذرية) إلى طاقة (مُقدَرة بالجول أو بوحدة المليون إلكترون فولت)
E = m C2 = 931 m
الطاقة بالجول تساوي حاصل ضرب الكُتلة بالكيلو جرام في مقدار ثابت (مُربع سرعة الضوء)، أو الطاقة بالمليون إلكترون فولت تساوي حاصل ضرب الكُتلة بوحدة الكُتل الذرية في مقدار ثابت (931).
إن البنية الذرية ظَلَّت وما زالت تشغلُ بال العُلماء بل وتحثُهم على بذل الجُهد في سبيل إكتشاف المزيد عنها ومعرفة أسرارها، ومِن ثَمَّ أخذت تبزُغ فروع جديدة في العلم حاملةً في طياتها مبادئ ونظريات تُحاول وَصف الكون بطريقة أفضل.
المصادر:
C.R. Nave (2006). HyperPhysics: Hydrogen Spectrum. Georgia State University. Accessed March 1st, 2008.
Dalton, John. “On the Absorption of Gases by Water and Other Liquids“, in Memoirs of the Literary and Philosophical Society of Manchester.
Andrew G. van Melsen (1952). From Atomos to Atom. Mineola, N.Y.: Dover Publications.
Miller PW et al. (2006) Chemical Communications 546-548.
Peter Atkins and Julio de Paula, Atkins’ Physical Chemistry, 8th edn (W.H. Freeman 2006), p.816-8.
Chmielewski, A.G. (2011). “Chemistry for the nuclear energy of the future”. Nukleonika.
Radiochemistry and Nuclear Chemistry; “Choppin, Liljenenzin and Rydberg”. ISBN 0-7506-7463-6, Butterworth-Heinemann.
Foundation for Chemistry. (n.d.). Retrieved from https://www.ck12.org/book/CK-12-Physical-Science-For-Middle-School/section/5.2/

