رغم أننا ناقشنا في المقال السابق من سلسلة مصادر الطاقة في الجسم – ولاسيما الجزء الخاص بالدهون – تحول الدهون الى احماض دهنية وكيتونات لغرض استهلاكها كطاقة، غير أن قضية الكيتون في الجسم بذاتها ما زالت تستحق الانتباه وما زال الكيتون يستحق المناقشة كأحد مصادر الطاقة في جسم الانسان.
أغلب من سمعوا بالكيتونات كانوا قد عرفوها من خلال الاطلاع على حمية الكيتو، وجانب من هؤلاء يعتقدون باقتصار عملية تنشئة الكيتونات (ketogenesis) في الجسم على هذه الحمية. الجانب الآخر من تناول قضية الكيتونات يأتي في سياق مناقشة حالات الطوارئ لمرضى السكري بنوعيه وبالأخص النوع الأول. حيث تنشئ حالة التحمض الكيتوني السكري نتيجة الارتفاع الحاد للسكر في الدم. وبين هاتين الحالتين هناك تساؤلات لدى بعض الناس حول كيفية سعينا لزيادة تنشئة الكيتونات في الحمية مع كونها خطراً يهدد الحياة عند ارتفاع السكر في الدم.
غير أن ما يغيب عن التساؤلات، هو كون تنشئة الكيتونات عملية تحدث بشكل يومي ودائم لدى الأشخاص الاعتياديين وحتى دون حمية، وكون ذلك مؤشراً على تفكيك الدهون في الجسم وهو ما نسعى له أولاً وأخيراً في الحمية. سنحاول في هذا المقال أن نغطي من الأسئلة ما يمكن أن يشرح عملية تنشئة الكيتونات في الجسم بأبسط شكل ممكن مثلما فعلنا في أجزاء السلسلة الأخرى حول:
ما هو الكيتون؟
الأجسام الكيتونية (ketone bodies) هي جزيئات قابلة للذوبان في الماء تحتوي على مجاميع كيتونية ناتجة من تفكيك الأحماض الدهنية في الكبد في العملية التي تعرف بتنشة الكيتونات (ketogenesis). والكيتونات بدورها هي مركبات تمتاز بوجود مستبدل كاربوني (مركبات تحتوي على الكاربون) وتضم مجموعة كربونيل (كربون واوكسجين بآصرة مزدوجة). أبسط الكيتونات هو الأسيتون، والمركب هذا معروف لإزالة صبغ الاظافر الذي تستخدمه النساء.
والاسيتون هذا سيظهر في احدى التحولات الكيميائية لتفكيك الدهون حتى انه يمكن شم رائحته إذ يقال لمرضى السكري أنه عند الارتفاع الحاد للسكر ستظهر رائحة شبيهة برائحة الأسيتون في زفيرهم. ومن الأمثلة الأخرى على المركبات الكيتونية لدينا السكريات، والكثير من المركبات الستيرويدية ومنها التستوستيرون نفسه. علينا إذاً أن نفصل بين الكيتون كنوع من المواد الكيميائية تشمل عدد كبير من المواد وبين الاجسام الكيتونية وهي ما سنتحدث عنه في هذا المقال.

الاسيتون المستخدم لإزالة صبغ الاظافر
كيف يحصل الجسم على الطاقة من الأجسام الكيتونية؟
لهذا السؤال عدة أوجه لكن أهمها الإجابة حول الآلية الكيميائية لاستفادة الجسم من الكيتونات. والاجابة ستكون جزءاً من نفس السؤال حول الدهون. مبدئياً فإننا نخزن الدهون في اجسامنا وكذلك نحصل عليها من الغذاء بشكل مباشر ولا حاجة للذكر بأن هذه الدهون لا تتعلق بالتغذية والطاقة فحسب بل تدخل في تكوين انسجة مهمة عديدة.
هناك صيغ عديدة لتداول الدهون في الجسم، لكن ما يتعلق بالطاقة منها هو الأحماض الدهنية (Fatty acids) حيث تصدر من الخلايا الدهنية الاحماض الدهنية الحرة (free fatty acids) مع انخفاض نسبة الانسولين وارتفاع الجلوكاغون. وتأتي الدهون من الغذاء أيضاً محمولة على البروتينات الدهنية التي نسمع بأسمائها كثيراً عندما نقوم بأجراء فحص كولسترول (LDL) و(VLDL) و(HDL) وهذه تحمل الدهون بأصناف مختلفة في الدم نحو الخلايا الدهنية بغرض خزنها. في نفس الظروف من انخفاض الانسولين وارتفاع الجلوكاغون فإن عملية تنشئة الكيتونات (Ketogenesis) ستتفعل.
قبل ذلك، ستحول عملية أكسدة بيتا الأحماض الدهنية الى المركب الهام والذي يعد وسيطاً نهائياً في عمليات الحصول على الطاقة من الدهون والكربوهيدرات، إنه اسيتيل مرافق الانزيم أ (Acetyl-CoA) (سنختصره اسيتيل م-أ) وتسمى العملية التي يتم تحويل الأحماض الدهنية فيها الى اسيتيل م-أ بأكسدة بيتا (beta oxidation)[1]. بعدها وبمساعدة العديد من الانزيمات، يتم تنشئة الاجسام الكيتونية[2]، والتي بدورها ستمر بطريقين، اما ان تستهلك بشكل مباشر كطاقة من قبل خلايا الدماغ التي تستطيع دون غيرها ان تستهلكها كطاقة لأن الاجسام الكيتونية تجتاز حاجز الدم-الدماغ (blood brain barrier) بكفاءة أكبر (هناك المزيد من التفاصيل حول هذا سنوضحها لاحقاً)، وكذلك خلايا القلب[3] فإنها تستطيع استهلاك الكيتونات فضلاً عن الأحماض الدهنية، الطريق الآخر هو أنها ستتحول الى اسيتيل م-أ ليذهب بدوره الى عمليات الحصول على الطاقة المألوفة. تعمل الكيتونات في خلايا الدماغ وفي القلب تماماً مثلما يعمل الجلوكوز.
ما نراه هنا هو أن الجسم قام بتحويل الأحماض الدهنية الى أسيتيل م-أ ثم عاد ليصنعه من الأجسام الكيتونية، فما الفائدة من ذلك؟ الفائدة الكبرى هي توفير الطاقة للدماغ والقلب في وقت يفتقر فيه الجسم لمصادر الطاقة الأخرى، إنه يبدو وكأنه وسيلة أخيرة لإنقاذ الجسم. بالتأكيد لا يعني ذلك أن من الممكن أن تنخفض نسبة السكر في الدم الى حد الصفر وان يعيش الانسان على الكيتون فقط، لكن ولحسن الحظ (أو لجودة عمليات الطاقة في جسمنا)، فإن ارتفاع الكيتونات وتفعيل مسار الطاقة المعتمد على تفكيك البروتين، الدهون، الكيتونات يفرز ظروفاً تعزز مقاومة الانسولين بشدة فيحتفظ الجسم بنسبة السكر لديه. نلاحظ حتى أنه عند الارتفاع الحاد في الكيتونات وفيما يعرف بالتحمض الكيتوني السكري أن الانسولين يكاد يفقد فاعليته، فتعطى لمرضى السكري تعليمات مختلفة تماما تتضمن تكثيف الجرعات وزيادتها بشكل كبير.
هذه اكثر إجابة مختصرة ممكنة حول كيفية الحصول على الطاقة من الكيتونات.
ما هي أنواع الكيتونات التي يصنعها الجسم؟
بعد تفكيك أسيتيل م-أ يصنع الجسم بمسارين مختلفين نوعين من المواد الكيتونية وهما حامض الاسيتو-اسيتيك المعروف أيضاً بالاسيتو الاسيتات (Acetoacetate)، والآخر هو حامض الهيدروكسي بيوتيريك-ب (β-Hydroxybutyric acid). عندما نسمع بالكيتونات في جسم الانسان فهاتان المادتان هما المقصودتان وهما كذلك المقصودتان عندما نتكلم عن الأجسام الكيتونية.
كل من هذين يمكن أن يتحولا الى المادة الأخرى، أي ان الاسيتو أسيتات يمكن ان تتحول الى هيدروكسي بيوتيريك – ب والعكس، وكلاهما يمكن ان يستخدما كطاقة من قبل الدماغ، ويمكن أيضاً أن يتحول الاسيتو اسيتات الى اسيتون أو الى اسيتيل م-أ. تتم هذه التحولات بمساعدة انزيمات معينة وبعضها دون الحاجة لانزيمات.
نلاحظ من هذا ان هناك مرونة كبيرة في التحولات الكيميائية، وكأن الجسم يريد الاستفادة من الطاقة مهما كلف الأمر وحيثما اقتضت الحاجة، فما يحتاجه الدماغ سيتم توفيره، ويمكن التلاعب بين الصيغ بحرية كبيرة.
هل تنشئة الكيتونات هي الطريقة الوحيدة التي يتم فيها تفكيك الدهون؟
كما اطلعنا، فإن تسمية الدهون يمكن أن تعني أشياء عدة، فعندما نتكلم عن الدهون في الجسم فهي ستتحرر الى احماض دهنية والتي سيشار اليها أيضاً بصفتها “دهون” وهي يمكن أن تستهلك كطاقة من العضلات بعد أن تتحول الى اسيتيل م-أ. وكذلك الدهون في الدم التي تحملها البروتينات الدهنية (lipoproteins) فهي أيضاً ترد بنفس الاصطلاح وتنتهي هذه بالخزن في الخلايا الدهنية، ولدينا أيضاً الدهون في الطعام التي تمر بتحولات عديدة وتنتهي أيضاً الى استهلاكها المباشر كأحماض دهنية من قبل العضلات، خزنها، أو تحويلها الى كيتونات.
باختصار، الجواب هو كلا، فهناك كما نرى ناتج آخر لتفكيك الدهون وليس فقط تحويلها الى كيتونات. (راجع بحث ناتاشا فيلمور في المصادر يُشرح فيه كيفية الحصول على الأدينوسين ثلاثي الفوسفات ATP من الأحماض الدهنية في ميتوكوندريا الخلايا).
كيف يمكن قياس الكيتونات في الدم؟
أولى تقنيات فحص الكيتون ظهرت في العام 1908 وكانت تعتمد على التفاعل الكيميائي مع حامض الهيدروكسيل الذي يخرج مع البول، غير أن التقنية لم تكن تقيس أي من الأجسام الكيتونية ولم تكن قادرة على ذلك. حمض الهيدروكسيل هو أحد النواتج التي تظهر في البول عند حدوث التحمض الكيتوني السكري لكن التقنية فيها الكثير من المعايب من حيث الوقت ومن حيث التطابق مع ما موجود في الدم من كيتونات وغير ذلك[4].
أما التقنية الدقيقة والشائعة فهي فحص الدم، والذي يقاس بأجهزة تقيس نسبة السكر أيضاً باستخدام شرائط مختلفة. هذه الأجهزة تستخدم بشكل رئيسي من قبل مرضى السكري وتحديداً عند حالات الارتفاع في سكر الدم، وتستخدم ايضاً في حالات الحمية لدى بعض الذين يريدون متابعة مدى فعالية فرط الكيتون لديهم عند الصيام أو مع حمية الكيتو.
وحدات قياس الكيتونات في أجهزة قياس الدم شبيهة بوحدات قياس سكر الدم وتقاس غالبا بوحدة الملي مول / لتر.
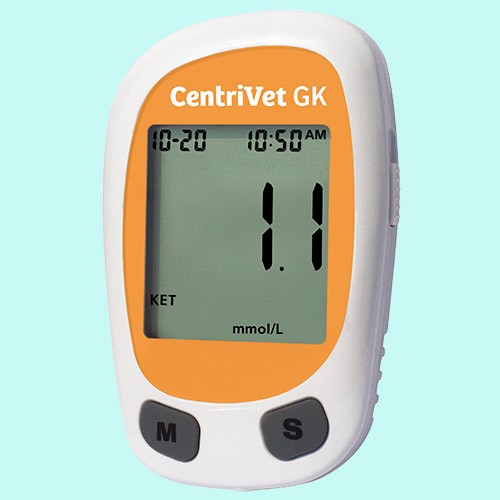
جهاز لقياس الكيتون في الدم
لماذا يكون ارتفاع الكيتونات خطيراً لدى مرضى السكري من النوع الأول؟
علينا أن نفرق بين فرط الكيتون (ketosis) وبين التحمض الكيتوني السكري (diabetic ketoacidosis). الفارق بين الاثنين يتجلى في مقدار ما يتم تحويله من اسيتيل م-أ الى كيتونات وبالتالي نسبة الكيتونات في الدم. مع ارتفاع الكيتونات الى درجة عالية تزداد حامضية الدم، وتقل كفاءة الانسولين حتى لا تعود الجرعات الاعتيادية تنفع، يكون الامر لاحقاً مصحوباً بألم في البطن ودوار وعطش شديد وتنفس مليء برائحة الاسيتون ثم يتبع حتى بأعراض دماغية مثل الهلوسات والشعور بالصدمة وقد ينتهي بتلف الأعضاء أو الوفاة.
تحدث الحالة لدى مرضى السكري كنتيجة لارتفاع السكر الذي يتلازم مع اعراض تزيد من ارتفاع السكر أكثر مثل تنشئة الجلوكوز في الكبد وإطلاق السكريات من الجلايكوجين وتفكيك الدهون وتنشئة الكيتونات. ويحدث ذلك غالباً مع حدوث مرض شديد او مع تناول الكثير من الكحول أو عند التعرض لإصابة شديدة أو في حالات الحمل، وأسباب أخرى.
أيهما أفضل للجسم الاعتماد على الاحماض الدهنية والكيتونات أم الاعتماد على الجلوكوز؟
يبدو مفاجئاً عندما نعلم أن الدماغ لا يعتمد على الأحماض الدهنية كطاقة بل على الكيتونات فقط. في بحثهما، ناقش بيتر شونفيلد وجورج ريسر هذا الأمر[5]. من الشائع أن الأحماض الدهنية لا تستطيع اجتياز الحاجز الدماغي الدموي (blood-brain barrier)، في حين تستطيع الكيتونات عبوره، لذا ففي ظروف شحة الجلوكوز في الجسم فإن أهمية الأجسام الكيتونية تتعاظم بالنسبة للدماغ. لكن هلا سألنا الدماغ عما يفضله من طاقة أولاً؟ هل يفضل الكيتونات أم الجلوكوز؟ لا يمكن اختصار الإجابة هنا فهناك الكثير من الأبحاث والمواضيع حول الأمر، والتي تناقشه من جوانب عدة منها ما يتعلق بالكفاءة ومنها ما يتعلق بالصحة على المدى الطويل. هل نسمع من العضلات ايضاً؟ ما الذي تفضله، الأحماض الدهنية أم الجلوكوز؟
يرى شونفيلد وزميله أن الدماغ يفضل الجلوكوز، وان السبب حول عدم قدرة الأحماض الدهنية على اجتياز الحاجز الدماغي الدموي غير دقيق، وأن السبب الأهم هو ان استهلاك الأحماض الدهنية له تأثيرات ضارة على الميتوكوندريا. فهو يفعل مسار الموت المبرمج للميتوكوندريا (راجع البودكاست مع علي البهادلي ونص الحوار المنشور في مجلة العلوم الحقيقية العدد 42 حول دور الميتوكوندريا في الموت المبرمج للخلايا). الإشكالية الثانية هي أن تكوين الادينوسين ثلاثي الفوسفات ATP من الاحماض الدهنية من أكسدة بيتا يتطلب المزيد من الاوكسجين وهذا يتسبب بنقص أكسجة الخلايا العصبية والذي يعد بحد ذاته مصدر ضرر للخلية وربما مسبب لموتها[6]. فضلاً عن أن مستوى الطاقة المتولدة أقل كفاءة مما يتولد عبر الاعتماد على الجلوكوز.
أما بالنسبة للعضلات، فهناك أيضاً مضار للاعتماد على الأحماض الدهنية كمصدر للطاقة بدلاً من الجلوكوز، يذكر أحد الأبحاث أنها تتسبب بزيادة مقاومة الانسولين في العضلات والخلايا القلبية كنتيجة لاستمرار الاعتماد على الاحماض الدهنية والمخلفات التي تنتج من هذا النمط من التغذية[7].
لا ننسى بالمقابل ضرورة هذه العمليات في التخلص من الدهون في الجسم، تخفيض السمنة وإزالة اعراض السكري من النوع الثاني[8] حتى كنتيجة للقيام بحمية كيتو متطرفة (التي يفترض أن تضر مقاومة الانسولين في العضلات). ليس من السهل الجزم بالفوائد والمضار عندما نقرأ أبحاثاً على المستوى الخلوي مثل هذه.
باختصار، لا يمكن تقديم إجابة واضحة عن “أيهما أفضل”، لكن من الواضح ربما أن الدماغ يفضل الجلوكوز، ومن الواضح أننا سنموت فوراً في حال أصبحت نسبة الجلوكوز في الجسم صفراً، لكننا لن نموت دون اكسدة الدهون أو تنشئة الكيتونات.
متى تحدث تنشئة الكيتونات في الجسم؟
مثل سائر عمليات الطاقة في الجسم، تحدث عمليات تنشئة الكيتونات بشكل مستمر ولكن بمعدلات متفاوتة. في الوضع الطبيعي قد تحدث بشكل منخفض جداً، وفي حالات أخرى قد تزداد.
كيف يمكن زيادة الكيتونات في الدم؟
عند الاطلاع على الأبحاث نجد أن الصيام هو الممارسة الأولى التي ترفع مستوى الكيتونات. لا حاجة للايضاح أن الصيام بالمفهوم العلمي لا يعني الصيام الإسلامي الذي يمنع تناول الماء وبالتالي فإن هذا قد يتسبب بوضع مختلف تماماً لكافة معادلات الطاقة في الجسم التي يعد الماء فيها محورياً. وجدت أبحاث أخرى أن القيام بالتمارين لفترات طويلة يتسبب أيضاً بزيادة تنشئة الكيتونات. كما وجد ان مرضى السكري لديهم نسبة أعلى بشكل عام من الكيتونات فيما لو قورنوا بالأشخاص الاعتياديين. يتلازم ايضاً مسار تنشئة السكريات من البروتينات مع مسار تفكيك الدهون وتنشئة الكيتونات في الجسم وكلاهما ينتجان من انخفاض نسبة الانسولين، ارتفاع الجلوكاغون والتي تتم اما عبر تقليل الكربوهيدرات أو قطعها أو قطع الطعام بشكل عام (الصيام).[9] [10]
ومن معايب الأبحاث التي اطلعنا عليها حول نسبة الكيتونات أن كثيراً منها أجري على مرضى السكري وأحد الأبحاث طلب من المشاركين عدم أخذ الانسولين لمدة 24 ساعة، وهذا سيزيد الكيتونات بشكل بديهي، كما ان تنشئة الكيتونات لا تختص بمرضى السكري دون غيرهم بل تحدث لدى الجميع ولا يصح تعميم ما لمرضى السكري على غيرهم. لكن ما يجري من أبحاث يتعلق ربما بخطورة الحالة التي يتعرض لها مرضى السكري دون غيرهم وهي التحمض الكيتوني.
هل ارتفاع الكيتونات خطير في حالة حمية الكيتو؟
لا حاجة للذكر أن فرط الكيتون لمرضى السكري لن يكون حالة طبيعية وسيترتب عليه تغيير في الجرعات. لكن ماذا عن الأشخاص الاعتياديين؟ تناقش المواقع الصحية الشهيرة مثل ويب مد، هيثل لاين، ومواقع أخرى مجموعة من المضار لفرط الكيتون. منها الخسارة العضلية، والتي تبدو بديهية لاسيما عندما نطلع على الجزء السابق في سلسلة مصادر الطاقة في جسم الانسان عن البروتين. لكن في الوقت نفسه، ليس هذا الأمر محسوماً ومثبتاً في الأبحاث، إنه فقط أمر يمكن أن نراه بديهياً، ولكن هناك احتمالات لعدم حدوثه أيضاً. لكن لو نقضنا الهدم العضلي فهل سيتحقق البناء العضلي بنفس الكفاءة؟ موضوع مطروح للبحث.
تذكر ايضاً هذه المواقع خطورة الجفاف كنتيجة لفرط الكيتون، لكن هذا ليس موضوعاً جديراً بالمناقشة في الابحاث بل يعتمد الأمر على العادات اليومية في شرب الماء.
فضلاً عن ذلك، يجب أن نعلم أن قضية مهمة مثل نمط الطاقة الذي يعتمد عليه الجسم هو أمر يمس كل خلية وكل نوع من الخلايا في الجسم ويتطلب الأمر لعدد لا يحصى من الأبحاث، لكن لا يجب أن ننظر له على أنه أمر “طبيعي” أو “تطورنا لنكون هكذا، لذا فهو طبيعي وجيد”، خصوصاً عندما نعلم أننا وبنظرتنا للصحة العامة ولمتوسط العمر في زمننا هذا فإننا نعيش ظروفاً لم يشهدها البشر من قبل. تطورت اجسامنا لتضمن لنا الطاقة في المجاعات وانعدام الغذاء وكنا نعيش بمتوسط عمر منخفض جداً، لكن اجسامنا ليست مؤهلة للإجابة عما سيضمن لنا حياة تزيد على 70 عاماً أو حياة دون سرطان أو غير ذلك من مسببات الوفاة الأكثر شيوعاً اليوم. هذه الأسئلة حديثة جداً بالنسبة لأجسام البشر التي تطورت لكي تبقى على قيد الحياة لمتوسط عمر 30 سنة.
ما هي النسبة الطبيعية للكيتونات في الدم؟
النسبة الطبيعية لمرضى السكري هي أقل من 0.6 ملي مول/لتر، أعلى من 1.6 يعتبر مؤشراً للخطر لمرضى السكري ويجدر بهم بعد ذلك مراقبة جرعات الانسولين.[11] للأشخاص الاعتياديين تتشابه النسب، ويهدف الأشخاص الذين يسعون لفرط الكيتون الى الحصول على نسب تفوق 1.5 أو على الأقل فوق الطبيعي 0.5.
المصادر
[1] Fillmore, Natasha, Osama Abo Alrob, and Gary D. Lopaschuk. “Fatty Acid beta-Oxidation.” AOCS Lipid library, doi 10 (2011).
[2] Dhillon, Kiranjit K., and Sonu Gupta. “Biochemistry, ketogenesis.” StatPearls [Internet] (2020).
[3] Kodde IF, van der Stok J, Smolenski RT, de Jong JW (January 2007). “Metabolic and genetic regulation of cardiac energy substrate preference”. Comp. Biochem. Physiol., Part a Mol. Integr. Physiol. 146 (1): 26–39. doi:10.1016/j.cbpa.2006.09.014. PMID 17081788
[4] Dhatariya, Ketan. “Blood ketones: measurement, interpretation, limitations, and utility in the management of diabetic ketoacidosis.” The review of diabetic studies: RDS 13.4 (2016): 217.
[5] Schönfeld, Peter, and Georg Reiser. “Why does brain metabolism not favor burning of fatty acids to provide energy?-Reflections on disadvantages of the use of free fatty acids as fuel for brain.” Journal of Cerebral Blood Flow & Metabolism 33.10 (2013): 1493-1499.
[6] Nieber, Karen. “Hypoxia and neuronal function under in vitro conditions.” Pharmacology & therapeutics 82.1 (1999): 71-86.
[7] Lopaschuk, Gary D. “Fatty acid oxidation and its relation with insulin resistance and associated disorders.” Annals of Nutrition and Metabolism 68.Suppl. 3 (2016): 15-20.
[8] Rogers, George W., et al. “Assessment of fatty acid beta oxidation in cells and isolated mitochondria.” Current protocols in toxicology 60.1 (2014): 25-3.
[9] Liljenquist, John E., et al. “Effects of glucagon on lipolysis and ketogenesis in normal and diabetic men.” The Journal of clinical investigation 53.1 (1974): 190-197.
[10] Sestoft, L., et al. “Regulation of gluconeogenesis and ketogenesis during rest and exercise in diabetic subjects and normal men.” Clinical science and molecular medicine 53.5 (1977): 411-418.
[11] NHS, Diabetic Ketoacidosis
مصادر أخرى:
Wikipedia, Ketone
Wikipedia, Ketone bodies
Wikipedia, Acetyl-CoA
Wikipedia, beta-Hydroxybutyric acid
Wikipedia, Beta Oxidation
Wikipedia, Fatty acid metabolism
