كتُب بواسطة: د. هبة محمود فوزي، مؤسسة موقع “سُكري \ Sukary“، طبيبة صيدلانية في مركز معلومات الأدوية، ومسؤولة عن يقظة وأمان الدواء.
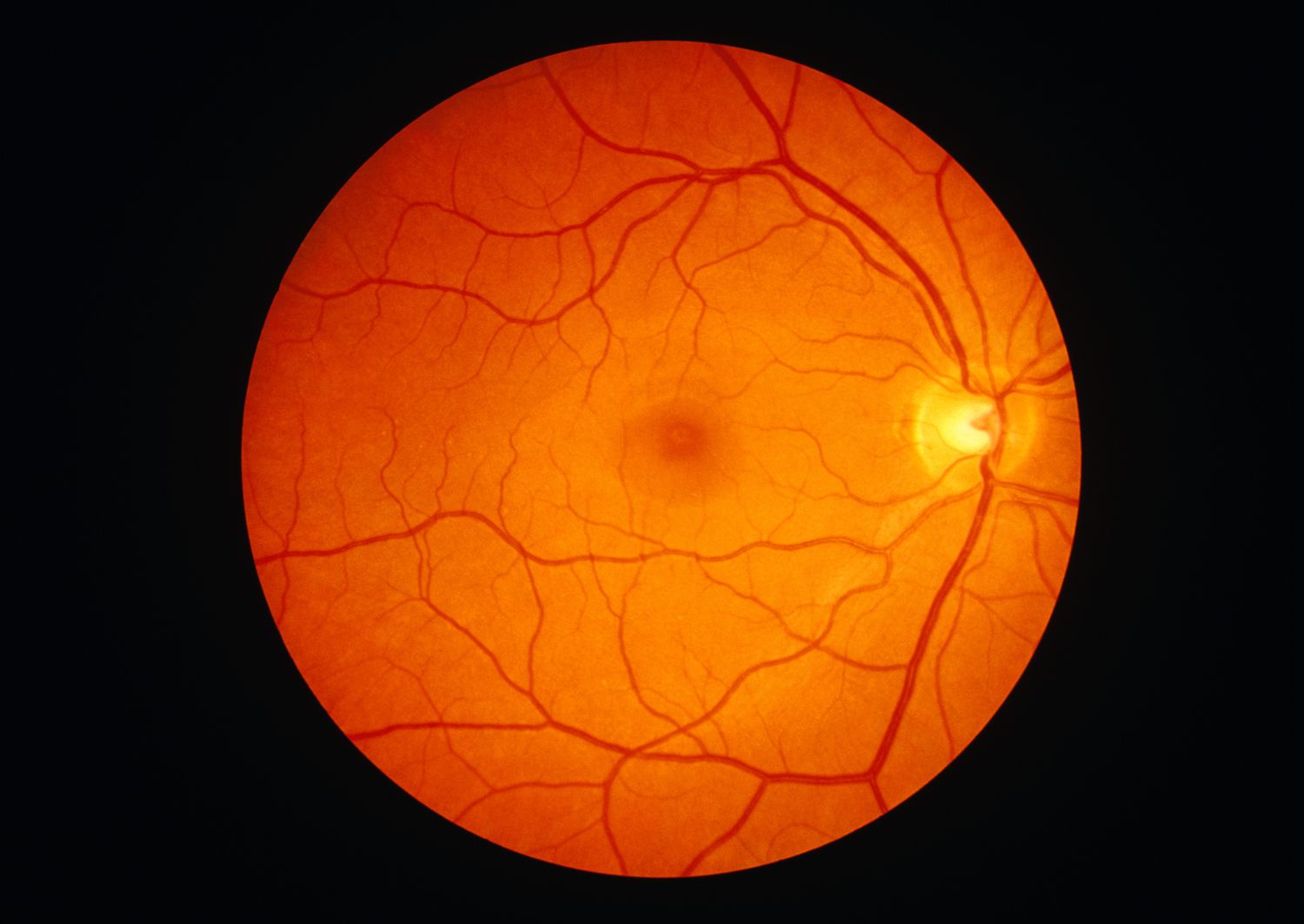
يُعَدّ اعتلال الشبكية السكري إحدى المضاعفات الخطيرة لداء السكري، ويتميز بحدوث اضطرابات وعائية دقيقة تؤدي إلى فقدان البصر غير القابل للعكس. و مع تزايد انتشار مرض السكري عالميًا، أصبح هذا الاعتلال محور اهتمام الأبحاث السريرية، نظرًا لتأثيره العميق على جودة حياة المرضى.
تشير الدراسات الوبائية الحديثة إلى أن عدد المصابين بالسكري عالميًا تجاوز 500 مليون شخص في عام 2021، مع توقعات بارتفاعه إلى 700 مليون بحلول عام 2045. و يُقدَّر أن نحو ثلث مرضى السكري معرضون للإصابة باعتلال الشبكية، مما يشير إلى تهديد صحي متزايد يستدعي تدابير علاجية ووقائية فعالة.
آلية تطور اعتلال الشبكية السكري
ينتج اعتلال الشبكية السكري نتيجة لارتفاع مستويات السكر في الدم لفترات طويلة دون ضبط كافٍ، مما يؤدي إلى تأثيرات ضارة على الأوعية الدموية الدقيقة وخلايا الشبكية. وتُعد هذه المضاعفات من الأسباب الرئيسية لفقدان البصر لدى مرضى السكري. نوضح هنا أهم الآليات البيولوجية المسؤولة عن هذا التلف، مع تبسيط المفاهيم للقارئ العام:
- الإجهاد التأكسدي: ما هو؟ وكيف يضر الشبكية؟
عند ارتفاع نسبة الجلوكوز في الدم لفترة طويلة، تبدأ الخلايا في إنتاج مركبات ضارة تُعرف باسم الجذور الحرة (Free Radicals) . هذه الجزيئات غير مستقرة وتهاجم مكونات الخلية مثل الغشاء والبروتينات والحمض النووي. في شبكية العين، و يؤدي هذا الهجوم إلى تدمير الخلايا البصرية ونمو أوعية دموية غير طبيعية وهشة.
متى تصبح الحالة خطيرة؟
يزداد خطر حدوث هذه الأضرار عندما يكون معدل السكر التراكمي (HbA1c) أعلى من 7% لفترة طويلة.
كيف يتجنب المريض هذا الخطر؟
- ضبط السكر التراكمي بمساعدة الطبيب.
- تناول أطعمة غنية بمضادات الأكسدة مثل فيتامين C (الحمضيات)، فيتامين E (المكسرات)، ومركبات البوليفينول (الشاي الأخضر، التوت).
- ممارسة التمارين بانتظام (30 دقيقة يوميًا).
- اختلال البروتينات مثل بروتين كيناز C
“بروتين كيناز C” هو إنزيم يتحكم في وظائف متعددة داخل الخلايا، ومنها تنظيم نفاذية الأوعية الدموية. وعند ارتفاع السكر، تنشط بعض الأنواع من هذا البروتين بشكل مفرط، مما يؤدي إلى:
- توسّع جدران الأوعية الدموية الدقيقة.
- زيادة تسرب السوائل داخل الشبكية.
- تورم البقعة الصفراء، وهي المنطقة المسؤولة عن الرؤية الدقيقة.
لماذا لا يشعر المريض مباشرة؟
هذا النوع من التلف لا يسبب ألمًا، بل يتطور بصمت، وقد يبدأ المريض بملاحظة غشاوة أو ضعف تدريجي في الرؤية لاحقًا.
كيفية الوقاية؟
- المتابعة السنوية عند طبيب العيون، حتى لو لم تظهر أعراض.
- ضبط ضغط الدم والكوليسترول لتقليل تأثير البروتينات المضطربة.
- الالتهاب الناتج عن مركبات AGEs
AGEs هي اختصار لـ Advanced Glycation End-products، وهي مركبات تتكوّن عندما ترتبط السكريات الزائدة بالبروتينات أو الدهون في الدم. و هذا التفاعل يعزز الالتهابات المزمنة في الأوعية، ويزيد من سماكتها وهشاشتها.
ما صلة هذه المركبات بالتحاليل؟
رغم أن AGEs لا تُقاس في التحاليل الدورية، إلا أن المستويات المرتفعة من:
- الدهون الثلاثية > 150 mg/dL
- LDL (الكوليسترول الضار) > 100 mg/dL تشير إلى بيئة مناسبة لتكوّن هذه المركبات.
كيفية الحد منها؟
- تناول طعام مطهو على البخار أو مشوي، وتجنب المقلي والمشوي على حرارة عالية.
- استخدام الدهون الصحية مثل زيت الزيتون.
- تقليل استهلاك السكر الأبيض والنشويات المكررة.
- السوربيتول: ما هو؟ وهل يجب تجنبه في الطعام؟
السوربيتول هو كحول سكري يتكوّن داخل الخلايا من الجلوكوز الزائد عن طريق إنزيم يُدعى ألدوّز ريدوكتاز. تراكم السوربيتول يؤدي إلى:
- سحب الماء إلى داخل الخلية.
- إحداث انتفاخ في خلايا الشبكية.
- تلف تدريجي للأوعية الدقيقة.
هل يجب تجنّب المنتجات التي تحتوي على سوربيتول؟
لا، السوربيتول الموجود في المنتجات الغذائية (مثل علكة الدايت) لا يُمثل خطرًا كبيرًا لأن كميته قليلة ويُمتص ببطء. الخطر الحقيقي هو الإنتاج الداخلي للسوربيتول بسبب ارتفاع الجلوكوز في الدم.
كيفية الوقاية؟
التحكم الصارم بمستوى الجلوكوز، خاصة بعد الوجبات، باستخدام:
- نظام غذائي منخفض المؤشر الجلايسيمي.
- الإفراط في إنتاج المواد المؤكسدة
المواد المؤكسدة، مثل بيروكسيد الهيدروجين وسوبر أكسيد، تُنتج في الجسم كجزء من عمليات الطاقة. لكن عند ارتفاع السكر المزمن، يزداد إنتاجها بشكل كبير، ما يؤدي إلى:
- تحفيز الالتهاب.
- تدمير الخلايا العصبية والأوعية الدموية الدقيقة.
ما أثرها على الشبكية؟
تُسهم هذه المواد في تدهور شبكية العين عبر إضعاف بنيتها وزيادة فرصة حدوث النزيف.
كيف نقلل إنتاجها؟
- تناول أغذية غنية بمضادات الأكسدة (مثل الخضروات الورقية، العنب الأحمر).
- تقليل تناول الأغذية المصنعة والمعلبة.
العوامل الوراثية والبيولوجية في اعتلال الشبكية السكري
لا يُعد اعتلال الشبكية السكري مجرد نتيجة لارتفاع السكر في الدم فقط، بل تشير الأبحاث الحديثة إلى أن العوامل الوراثية تلعب دورًا جوهريًا في تحديد من هم أكثر عرضة للإصابة بهذا المضاعف من بين مرضى السكري. إذ تختلف استجابة الأشخاص لارتفاع السكر، باختلاف تركيبتهم الجينية. بعض الجينات المرتبطة بهذا المرض تم تحديدها من خلال دراسات جينية واسعة النطاق (GWAS)، وقد تبيّن أن بعض التغيرات (الطفرات أو التعديلات) فيها ترتبط بدرجة أعلى من خطر تطور المرض، خاصة في المراحل المتقدمة. من أبرز هذه الجينات:
- جين نمو بطانة الأوعية الدموية VEGF (Vascular Endothelial Growth Factor):
هذا الجين مسؤول عن إنتاج بروتين يحفّز تكوّن أوعية دموية جديدة. في الحالات الطبيعية، و يُعد وجود VEGF مفيدًا في التئام الجروح وتحفيز النمو الدموي. لكن في الشبكية السكّرية، يؤدي ارتفاع مستويات هذا البروتين إلى:
- نمو أوعية دموية جديدة غير طبيعية وضعيفة، تنمو داخل الشبكية أو على سطحها.
- تمزق أو نزيف هذه الأوعية بسهولة، مما يؤدي إلى تلف الرؤية وربما انفصال الشبكية في الحالات الشديدة.
و تجدر الإشارة إلى أن بعض الأشخاص الذين يحملون طفرات في جين VEGF من الممكن أن يحدث لهم إنتاج مفرط للبروتين، ما يضاعف خطر الإصابة بمضاعفات الشبكية بنسبة تصل إلى 30-40% مقارنة بغيرهم من مرضى السكري .
- جين تحريض الالتهابات في الجسم TNF-α (Tumor Necrosis Factor-alpha):
هو جين ينتج بروتينًا يُعتبر من أقوى محرضات الالتهاب في الجسم. عندما يكون مفعوله مفرطًا:
- يُحدث التهابًا مزمنًا في الأوعية الدموية الدقيقة للشبكية.
- يزيد من نفاذية الأوعية وتسرب السوائل.
- يسرّع من تدهور الشبكية وتلف الأعصاب البصرية.
🔍 أظهرت دراسات Khan et al., Cytokine, 2019 أن وجود تعدد شكلي معين (polymorphism) في هذا الجين مرتبط بزيادة خطر اعتلال الشبكية، خصوصًا لدى مرضى السكري من النوع الثاني.
- جين تنظيم انتاج اوكسيد النتريك eNOS (Endothelial Nitric Oxide Synthase):
هذا الجين ينظّم إنتاج أكسيد النيتريك (NO)، وهو مركب يساعد على توسّع الأوعية الدموية وضمان تدفق الدم بشكل سلس. لكن عند وجود خلل في هذا الجين:
- يقل إنتاج أكسيد النيتريك.
- تتقلّص الأوعية الدموية بشكل غير طبيعي.
- يقل تروية الشبكية، مما يساهم في نقص الأوكسجين (نقص التروية)، وهو عامل رئيسي في تحفيز نمو أوعية دموية ضارة كما في حالة VEGF
وُجد أن بعض الطفرات في هذا الجين تؤدي إلى نشاط أقل بنسبة تصل إلى 60% من الطبيعي، وتزيد احتمالية اعتلال الشبكية خصوصًا في المرضى ذوي الضغط المرتفع المصاحب للسكري.
- جين تحويل الجلوكوز الزائد الى سوربيتول AKR1B1 (Aldo-Keto Reductase Family 1 Member B1):
هذا الجين يرمّز لإنزيم يُحوّل الجلوكوز الزائد إلى سوربيتول، وهو ما ذكرناه سابقًا كمسبب لتلف الخلايا الشبكية. عند وجود طفرة في هذا الجين:
- يُنتَج السوربيتول بمعدلات أعلى.
- تتفاقم ظاهرة الإجهاد التأكسدي والالتهاب داخل العين.
وُجدت بعض الطفرات في هذا الجين بشكل أكثر شيوعًا في مجتمعات آسيوية وشرق أوسطية، مع ارتباط ملحوظ بزيادة خطر اعتلال الشبكية بمقدار 1.5 إلى 2 ضعف مقارنة بغير الحاملين للطفرات.
- جين ارتباط السكر الزائد بالبروتينات RAGE (Receptor for Advanced Glycation End-products):
هذا الجين يُنتج مستقبلات لبروتينات AGEs، وهي مركبات تتكوّن كما شرحنا سابقًا نتيجة ارتباط السكر الزائد بالبروتينات. في الحالات العادية، توجد هذه المستقبلات بمستويات منخفضة. لكن عند زيادة تعبير جين RAGE:
- تتضخم الاستجابة الالتهابية لمركبات AGEs.
- تزداد تفاعلات الإجهاد التأكسدي وتلف الأوعية.
- يتحول الوضع إلى حلقة مفرغة من الالتهاب وتلف الأنسجة.
أظهرت دراسات وراثية وجود علاقة بين التعبير العالي لجين RAGE وتطور اعتلال الشبكية في مراحل مبكرة ومتقدمة لدى مرضى النوع الثاني .[i]
مراحل اعتلال الشبكية السكري
يمر المرض بمرحلتين رئيسيتين:
- المرحلة غير التكاثرية:و فيها تتلف الأوعية الدموية الصغيرة، مما يؤدي إلى تسرب السوائل وتكوين انتفاخات صغيرة في الشعيرات الدموية.
- المرحلة التكاثرية: تنمو أوعية دموية جديدة ضعيفة وسهلة التمزق، مما قد يؤدي إلى نزيف داخل العين، تكوّن أنسجة ليفية، أو انفصال الشبكية، ما يؤدي إلى فقدان البصر.
دور الميتوكوندريا في اعتلال الشبكية السكري
الميتوكوندريا هي “محطات الطاقة” داخل الخلايا، حيث يتم إنتاج أغلب جزيئات الطاقة التي تحتاجها الخلية لتعمل، وخاصة في الخلايا النشطة مثل خلايا شبكية العين. لكن في حالة السكري المزمن، تتعرض هذه العضيات الحيوية لسلسلة من الاضطرابات التي تساهم بشكل كبير في تطور اعتلال الشبكية السكري.
كيف يتأثر أداء الميتوكوندريا بارتفاع السكر في الدم؟
عندما تبقى مستويات الجلوكوز مرتفعة لفترات طويلة، تدخل كميات كبيرة منه إلى الخلايا، وتُجبَر الميتوكوندريا على “حرق” هذا الجلوكوز لإنتاج الطاقة. هذه الزيادة المفرطة في النشاط تُنتج كمية زائدة من الجذور الحرة (Reactive Oxygen Species – ROS) وهي جزيئات شديدة التفاعل تدمّر مكونات الخلية إن لم تُحيد بسرعة.
لكن مع مرور الوقت:
- تُصاب الميتوكوندريا نفسها بالتلف، وخاصة حمضها النووي الداخلي (mtDNA)، الذي يفتقر لآليات إصلاح متطورة كما في نواة الخلية.
- ينخفض كفاءة إنتاج الطاقة، وتُصبح الخلية أكثر عرضة للتلف.
- تتزايد دورة الإجهاد التأكسدي المزمن، مما يؤدي إلى دمار تدريجي في خلايا الشبكية الحساسة للضوء والأوعية الدموية المغذية لها.
لماذا هذا الدور مهم في الشبكية تحديدًا؟
شبكية العين من أكثر أنسجة الجسم استهلاكًا للأكسجين والطاقة. لذلك، أي خلل في عمل الميتوكوندريا فيها يؤدي بسرعة إلى:
- ضعف في أداء الخلايا البصرية.
- موت الخلايا العصبية الشبكية (Apoptosis).
- تحفيز الالتهاب ونمو أوعية دموية غير طبيعية كرد فعل على “نقص الطاقة” وتضرر البيئة الداخلية.
و قد أظهرت دراسات عدة[ii] أن الفئران المصابة بالسكري تظهر تغيرات واضحة في بنية ووظيفة الميتوكوندريا في الشبكية خلال أسابيع من ارتفاع السكر، مما يسبق ظهور الأعراض العينية السريرية.
التغيرات الخلوية والجزيئية التي تحدث في حالة اعتلال الشبكية السكري
- تلف الخلايا البطانية للأوعية الدموية: اعتلال الشبكية السكري يؤثر على الأوعية الدموية الدقيقة في الشبكية، مما يؤدي إلى:
- زيادة النفاذية، مما يسمح بتسرب السوائل والبروتينات.
- ضعف قدرة الخلايا البطانية على التجدد.
- زيادة التصاق خلايا الدم البيضاء بجدران الأوعية، مما يسبب التهابات إضافية.
- التغيرات في المادة خارج الخلوية (ECM – Extracellular Matrix):
عند ارتفاع السكر في الدم لفترة طويلة، تتراكم مركبات سكرية ضارة تُعرف بـ”AGEs” (Advanced Glycation End Products – المنتجات النهائية لارتباط السكر بالبروتينات)، داخل الأنسجة المحيطة بالأوعية الدموية. و هذا يؤدي إلى زيادة سماكة الغشاء القاعدي، وهو طبقة دقيقة تدعم الأوعية، مما يجعلها أقل مرونة ويضعف تدفق الدم داخل الشبكية، ويزيد من خطر تلف خلايا العين.
- التنكس العصبي الشبكي: يسبب السكري تلفًا في الخلايا العصبية في الشبكية، حتى قبل ظهور الأعراض السريرية، ويؤدي إلى ضعف الرؤية تدريجيًا. بالإضافة إلى ذلك، يقل تزويد الأوعية الدموية بالأوكسجين، مما يتسبب في تلف الخلايا العصبية.
اعتلال الشبكية السكري: مناهج علاجية جديدة تستهدف آليات الأكسدة والمناعة
العلاجات الحالية لاعتلال الشبكية السكري
تعتمد العلاجات المتاحة حاليًا على تقليل تدهور حالة الشبكية، ولكنها لا تحقق الشفاء التام. و تشمل هذه العلاجات:
- التحكم بمستويات السكر وضغط الدم: يساعد في تقليل تدهور حالة الشبكية بشكل عام، لكنه لا يعكس الأضرار التي حدثت بالفعل.
- العلاج بالليزر (التخثير الضوئي للشبكية): يستخدم للتقليل من نمو الأوعية الدموية غير الطبيعية التي قد تؤدي إلى النزيف أو تلف الشبكية، ولكنه قد يؤثر على الرؤية المحيطية.
- الحقن داخل العين بمثبطات VEGF: تُستخدم للحد من نمو الأوعية الدموية غير الطبيعية في الشبكية، ولكنها لا تمنع تطور المرض تمامًا.
- استئصال الجسم الزجاجي: ُيستخدم في حالات النزيف الشديد أو انفصال الشبكية المتقدم.
- العلاج بالستيرويدات داخل العين: يساعد في تقليل الالتهاب في الشبكية، ولكنه قد يزيد من خطر الإصابة ببعض المشاكل مثل المياه الزرقاء (الجلوكوما) أو إعتام العدسة.
العلاجات الحديثة في دراسة جديدة
في دراسة حديثة نُشرت تحت عنوان اعتلال الشبكية السكري[iii]: مناهج علاجية جديدة تستهدف آليات الأكسدة والمناعة صدرت من قسم طب العيون في المركز الطبي الجامعي بجامعة يوهانس جوتنبرج في ماينز، ألمانيا. و نشرت في مجلة Antioxidants في العدد 13، المجلد 5، بتاريخ 12 مايو 2024. تم التركيز على استراتيجيات علاجية مبتكرة تهدف إلى معالجة آليات الأكسدة والمناعة التي تلعب دورًا كبيرًا في تطور المرض. و تم اقتراح علاجات جديدة تعتمد على التعامل مع الإجهاد التأكسدي (أي التلف الذي تسببه الجذور الحرة في الخلايا) والتفاعلات المناعية غير الطبيعية التي تحدث في الشبكية. و هذه العلاجات تهدف إلى:
- تقليل التأثيرات السلبية للإجهاد التأكسدي: من خلال استخدام مضادات الأكسدة التي تساعد في حماية خلايا الشبكية من التلف الناتج عن الجذور الحرة.
- تقليل الالتهابات: حيث يُعتقد أن الالتهابات المزمنة تساهم في تدهور الأوعية الدموية في الشبكية. من خلال تقليل الالتهابات، يمكن تحسين وظيفة الأوعية الدموية في العين.
دور مضادات الأكسدة في العلاج
بما أن الإجهاد التأكسدي من العوامل الرئيسية التي تساهم في تلف الشبكية لدى مرضى السكري عن طريق عمل الجسم على تكوين جزيئات تُسمى الجذور الحرة التي تضر بالخلايا. لذا، فإن استخدام مضادات الأكسدة يعد من العلاجات الواعدة التي قد تساعد في الوقاية من هذا التلف.
- مضادات الأكسدة الطبيعية والصيدلانية: مثل اللوتين والريسفيراترول، التي تساهم في تقليل التلف العصبي والالتهابات في الشبكية.
- الإنزيمات المضادة للأكسدة:
أحد الإنزيمات الأساسية في خلايا الجسم هو “سوبر أوكسيد ديسموتاز” (Superoxide Dismutase)، وهو إنزيم لا نتحدث عنه كثيرًا، رغم أن وظيفته حيوية للغاية؛ حيث يساهم في تحييد الجذور الحرة الضارة داخل الخلية، وهي جزيئات تتسبب في تلف الخلايا عند تراكمها، خاصة في شبكية العين لدى مرضى السكري. ورغم أهميته، لا يُستخدم هذا الإنزيم كدواء مباشر، ولا توجد طريقة فعالة حاليًا لحقنه أو زيادته بشكل مباشر داخل الجسم. لكن بعض الدراسات تشير إلى أن اتباع نمط حياة صحي مثل ممارسة الرياضة بانتظام وتناول أطعمة غنية بمضادات الأكسدة (كالخضروات الورقية والتوت والمكسرات) قد يُحفّز الجسم على إنتاجه بشكل طبيعي. الفكرة هنا ليست استخدامه كعلاج، بل دعم دفاعات الجسم الذاتية ضد الضرر التأكسدي الذي يلعب دورًا في اعتلال الشبكية السكري.
المستقبل في العلاج
البحث في هذه العلاجات الجديدة يعد واعدًا للغاية، حيث يُتوقع أن توفر استراتيجيات مثل مضادات الأكسدة وتقنيات استهداف الأكسدة والمناعة وسائل أكثر فعالية لإبطاء تطور اعتلال الشبكية السكري وتحسين جودة حياة المرضى. ومع ذلك، لا تزال هناك حاجة إلى مزيد من الدراسات لتقييم مدى فعالية هذه العلاجات على المدى الطويل.
من خلال هذه المناهج العلاجية الجديدة، يأمل الباحثون في تقديم حلول مبتكرة وأكثر فعالية لمكافحة اعتلال الشبكية السكري، وتحسين فرص الحفاظ على الرؤية لدى المرضى المصابين.
مراجع
[i] Mishra, R. et al. (2016). Rage gene promoter polymorphisms and diabetic retinopathy in a clinic-based population from South India. Eye, 30(10), 1393–1398. https://www.nature.com/articles/eye2016155
[ii]Kowluru, R. A. (2019). Mitochondrial Stability in Diabetic Retinopathy: Lessons Learned From Epigenetics. Diabetes, 68(2), 241–247.
[iii] Diabetic Retinopathy: New Treatment Approaches Targeting Redox and Immune Mechanisms